Nomenclatura, tipos, propriedades e exemplos de óxidos
O óxidos eles são uma família de compostos binários onde há interações entre o elemento e o oxigênio. Portanto, um óxido tem uma fórmula muito geral do tipo EO, em que E é qualquer elemento.
Dependendo de muitos fatores, como a natureza eletrônica de E, seu raio iônico e suas valências, vários tipos de óxidos podem ser formados. Alguns são muito simples e outros, como Pb3O4, (chamado minium, arcazón ou chumbo vermelho) são misturados; isto é, eles resultam da combinação de mais de um óxido simples.

Mas a complexidade dos óxidos pode ir mais longe. Existem misturas ou estruturas nas quais mais de um metal pode intervir, e onde além disso as proporções não são estequiométricas. No caso do Pb3O4, a relação Pb / O é igual a 3/4, dos quais tanto o numerador quanto o denominador são inteiros.
Em óxidos não estequiométricos, as proporções são números decimais. Oe0.75O1.78, é um exemplo de um óxido não-estequiométrico hipotético. Este fenômeno ocorre com os chamados óxidos metálicos, especialmente com os metais de transição (Fe, Au, Ti, Mn, Zn, etc.).
No entanto, existem óxidos cujas características são muito mais simples e diferenciáveis, assim como o caráter iônico ou covalente. Nos óxidos em que predomina o caráter iônico, eles serão compostos de cátions E+ e aniões O2-; e aquelas ligações puramente covalentes, simples (E-O) ou duplas (E = O).
O que dita o caráter iônico de um óxido é a diferença na eletronegatividade entre E e O. Quando E é um metal muito eletropositivo, então OE terá um alto caráter iônico. Enquanto se E é eletronegativo, a saber, um não-metal, seu óxido EO será covalente.
Esta propriedade define muitos outros exibidos pelos óxidos, assim como sua capacidade de formar bases ou ácidos em solução aquosa. A partir daqui surgem os chamados óxidos básicos e ácidos. Aqueles que não se comportam como um dos dois, ou que ao contrário manifestam ambas as características, são óxidos neutros ou anfotéricos.
Índice
- 1 nomenclatura
- 1.1 Nomenclatura sistemática
- 1.2 Nomenclatura de ações
- 1.3 Nomenclatura Tradicional
- 2 tipos de óxidos
- 2.1 óxidos básicos
- 2.2 Óxidos Ácidos
- 2.3 Óxidos Neutros
- 2.4 Óxidos Anfotéricos
- 2.5 óxidos mistos
- 3 Propriedades
- 4 Como eles são formados?
- 5 exemplos de óxidos
- 5.1 óxidos metálicos de transição
- 5.2 Exemplos adicionais
- 6 referências
Nomenclatura
Existem três maneiras de mencionar os óxidos (que também se aplicam a muitos outros compostos). Estes são corretos, independentemente do caráter iônico do óxido de óxido de etileno, de modo que seus nomes não dizem nada sobre suas propriedades ou estruturas.
Nomenclatura sistemática
Dado os óxidos EO, E2O, E2O3 e EO2À primeira vista, o que está por trás de suas fórmulas químicas não pode ser conhecido. No entanto, os números indicam as proporções estequiométricas ou a relação E / S. A partir desses números, eles podem receber nomes, embora não seja especificado com qual valência "funciona" E.
Os números de átomos para E e O são indicados pelos prefixos de números gregos. Desta forma, mono- significa que existe apenas um átomo; di, dois átomos; tri-, três átomos e assim por diante.
Então, os nomes dos óxidos anteriores de acordo com a nomenclatura sistemática são:
-MonóÓxido E (EO).
-Monóxido diE (E2O)
-Trióxido de diE (E2O3).
-DiE óxido (EO2).
Aplicando então esta nomenclatura para o Pb3O4, o óxido vermelho da primeira imagem, temos:
Pb3O4: tetraóxido de triChumbo
Para muitos óxidos mistos, ou com altas taxas estequiométricas, é muito útil recorrer à nomenclatura sistemática para nomeá-los.
Nomenclatura de ações
Valencia
Embora não se saiba qual elemento é E, é suficiente com a relação E / S saber qual a valência que ele está usando em seu óxido. Como? Através do princípio da eletroneutralidade. Isso requer que a soma das cargas dos íons em um composto seja igual a zero.
Isso é feito assumindo um alto caráter iônico para qualquer óxido. Assim, o O tem carga -2 porque é O2-e E deve fornecer n + para neutralizar as cargas negativas do ânion óxido.
Por exemplo, no EO o átomo E trabalha com valência +2. Por quê? Porque senão não poderia neutralizar a carga -2 do único O. Para o E2Ou, o E tem valência +1, pois a carga +2 deve ser dividida entre os dois átomos de E.
E no E2O3, deve ser calculado primeiro os encargos negativos contribuídos pelo O. Como são três deles, então: 3 (-2) = -6.Para neutralizar a carga -6 é necessário que o E forneça +6, mas como há dois deles, +6 é dividido por dois, deixando E com uma valência de +3.
Regra mnemônica
O sempre tem a valência -2 nos óxidos (a menos que seja um peróxido ou superóxido). Assim, uma regra mnemônica para determinar a valência de E é simplesmente levar em conta o número que acompanha o O. E, por sua vez, terá o número 2 acompanhando-o, e se não, significa que houve uma simplificação.
Por exemplo, em EO a valência de E é +1, porque mesmo que não esteja escrito, há apenas um O. E para o EO2, como não há 2 E de acompanhamento, houve uma simplificação, e para fazer parecer que deve ser multiplicado por 2. Assim, a fórmula permanece como E2O4 e a valência de E é então +4.
No entanto, essa regra falha para alguns óxidos, como Pb3O4. Portanto, é sempre necessário realizar os cálculos de neutralidade.
Em que consiste
Uma vez tendo a valência de E à mão, a nomenclatura das ações consiste em especificá-la entre parênteses e com algarismos romanos. De todas as nomenclaturas, esta é a mais simples e precisa no que diz respeito às propriedades eletrônicas dos óxidos.
Se E, por outro lado, tiver apenas uma valência (que pode ser encontrada na tabela periódica), então ela não é especificada.
Assim, para o óxido EO se E tem valência +2 e +3, é chamado: óxido de (nome de E) (II). Mas se E só tem valência +2, então seu óxido é chamado: óxido (nome de E).
Nomenclatura tradicional
Para mencionar o nome dos óxidos, os sufixos -ico ou -oso, para as valências maiores ou menores, devem ser adicionados aos seus nomes latinos. Caso haja mais de dois, então os prefixos -hype, para o menor e -per, para o maior de todos-são usados.
Por exemplo, o chumbo trabalha com valências +2 e +4. No PbO tem valência +2, por isso é chamado: óxido plumboso. Enquanto o PbO2 É chamado: óxido plumico.
E o Pb3O4como é chamado de acordo com as duas nomenclaturas anteriores? Não tem nome. Por quê? Porque o Pb3O4 na verdade consiste em uma mistura 2 [PbO] [PbO2]; isto é, o sólido vermelho tem uma concentração dupla de PbO.
Por esta razão, seria errado tentar dar um nome ao Pb3O4 isso não consiste na nomenclatura sistemática ou na gíria popular.
Tipos de óxidos
Dependendo de qual parte da tabela periódica é E e, portanto, sua natureza eletrônica, um tipo de óxido ou outro pode ser formado. Daqui vários critérios surgem para atribuir-lhes um tipo, mas os mais importantes são aqueles relacionados à sua acidez ou basicidade.
Óxidos básicos
Os óxidos básicos são caracterizados por serem iônicos, metálicos e, mais importantes, gerando uma solução básica quando dissolvidos em água. Para determinar experimentalmente se um óxido é básico, ele deve ser adicionado a um recipiente com água e indicador universal dissolvido nele. Sua coloração antes de adicionar o óxido deve ser verde, pH neutro.
Uma vez que o óxido é adicionado à água, se sua cor muda de verde para azul, isso significa que o pH se tornou básico. Isso porque estabelece um equilíbrio de solubilidade entre o hidróxido formado e a água:
EO (s) + H2O (l) => E (OH)2(s) <=> E2+(ac) + OH-(ac)
Embora o óxido seja insolúvel em água, é suficiente que uma pequena porção se dissolva para modificar o pH. Alguns óxidos básicos são tão solúveis que geram hidróxidos cáusticos como NaOH e KOH. Ou seja, os óxidos de sódio e potássio, Na2O e K2Ou são muito básicos. Observe a valência de +1 para ambos os metais.
Óxidos Ácidos
Os óxidos ácidos são caracterizados por terem um elemento não metálico, são covalentes e também geram soluções ácidas com água. Mais uma vez, a sua acidez pode ser verificada com o indicador universal. Se desta vez, adicionando o óxido à água, sua cor verde fica avermelhada, então é um óxido de ácido.
Que reação acontece? A seguinte:
EO2(s) + H2O (l) => H2EO3(ac)
Um exemplo de um óxido de ácido, que não é um sólido, mas um gás, é CO2. Quando se dissolve em água, forma ácido carbônico:
CO2(g) + H2O (l) <=> H2CO3(ac)
Da mesma forma, o CO2 Não consiste em ânions O2- e C cátions4+mas em uma molécula formada por ligações covalentes: O = C = O. Esta é talvez uma das maiores diferenças entre óxidos e ácidos básicos.
Óxidos Neutros
Esses óxidos não alteram a cor verde da água em pH neutro; isto é, não formam hidróxidos nem ácidos em solução aquosa. Alguns deles são: N2O, NO e CO. Como o CO, eles têm ligações covalentes que podem ser ilustradas pelas estruturas de Lewis ou por qualquer teoria de ligação.
Óxidos anfotéricos
Outra maneira de classificar os óxidos depende se eles reagem com um ácido ou não.A água é um ácido muito fraco (e também uma base), então os óxidos anfotéricos não exibem "ambos os lados". Estes óxidos são caracterizados por reagir com ácidos e bases.
O óxido de alumínio, por exemplo, é um óxido anfotérico. As duas equações químicas a seguir representam sua reação com ácidos ou bases:
Al2O3(s) + 3H2SO4(ac) => Al2(SO4)3(ac) + 3H2O (l)
Al2O3(s) + 2NaOH (ac) + 3H2O (l) => 2NaAl (OH)4(ac)
Al2(SO4)3 é o sal sulfato de alumínio e NaAl (OH)4 um sal complexo chamado aluminato tetrahidroxial de sódio.
Óxido de hidrogênio, H2Ou (água), também é anfotérico, e isso é evidenciado em seu equilíbrio de ionização:
H2O (l) <=> H3O+(ac) + OH-(ac)
Óxidos mistos
Óxidos mistos são aqueles que consistem da mistura de um ou mais óxidos no mesmo sólido. O Pb3O4 É um exemplo deles. A magnetita, Faith3O4, também é outro exemplo de um óxido misto. A fé3O4 É uma mistura de FeO e Fe2O3 em proporções de 1: 1 (ao contrário de Pb)3O4).
As misturas podem ser mais complexas, originando assim uma rica variedade de minerais óxidos.
Propriedades
As propriedades dos óxidos dependem do seu tipo. Os óxidos podem ser iônicos (En +O2-), como CaO (Ca2+O2-), ou covalente, como SO2, O = S = O.
A partir deste fato, e da tendência dos elementos de reagirem com ácidos ou bases, várias propriedades são coletadas para cada óxido.
Além disso, o acima é refletido nas propriedades físicas, como pontos de fusão e ebulição. Os óxidos iônicos tendem a formar estruturas cristalinas muito resistentes ao calor, então seus pontos de fusão são altos (acima de 1000 ° C), enquanto o covalente derrete a baixas temperaturas, ou mesmo gases ou líquidos.
Como eles são formados?
Óxidos são formados quando os elementos reagem com o oxigênio. Essa reação pode ocorrer com simples contato com atmosferas ricas em oxigênio, ou requer calor (como a chama de um isqueiro). Ou seja, quando um objeto é queimado, ele reage com o oxigênio (desde que esteja presente no ar).
Se uma parte de fósforo é retirada, por exemplo, e colocada na chama, ela queimará e formará o óxido correspondente:
4P (s) + 5O2(g) => P4O10(s)
Durante este processo, alguns sólidos, como o cálcio, podem queimar com uma chama brilhante e colorida.
Outro exemplo é obtido pela queima de madeira ou qualquer substância orgânica, que possui carbono:
C (s) + O2(g) => CO2g)
Mas se houver uma insuficiência de oxigênio, CO é formado em vez de CO2:
C (s) + 1 / 2O2(g) => CO (g)
Observe como a relação C / O é usada para descrever diferentes óxidos.
Exemplos de óxidos
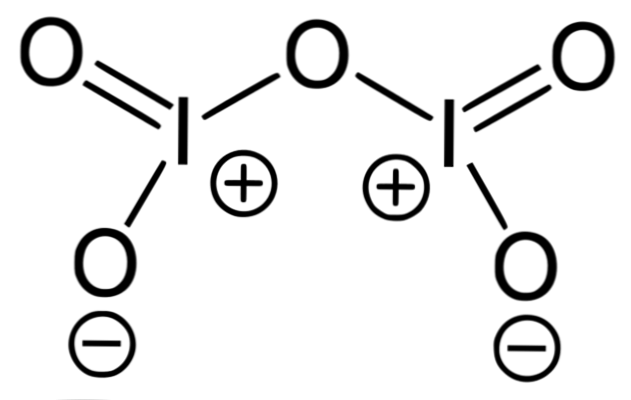
A imagem superior corresponde à estrutura de óxido covalente I2O5, a forma mais estável de iodo. Note suas ligações simples e duplas, bem como as cargas formais de eu e oxigênio para seus lados.
Os óxidos de halogênio são caracterizados por serem covalentes e muito reativos, como são os casos de O2F2 (F-O-O-F) e OF2 (F-O-F). Dióxido de cloro, ClO2, por exemplo, é o único óxido de cloro sintetizado em escala industrial.
Como os halogênios formam óxidos covalentes, suas valências "hipotéticas" são calculadas da mesma forma pelo princípio da eletroneutralidade.
Óxidos de metal de transição
Além dos óxidos de halogênio, temos os óxidos dos metais de transição:
-CoO: óxido de cobalto (II); óxido de cobalto; monóxido de cobalto.
-HgO: óxido de mercúrio (II); óxido mercúrico; u monóxido de mercúrio.
-Ag2O: óxido de prata; óxido de prata; ou monóxido de diplata.
-Au2O3: óxido de ouro (III); óxido aureico; ou trióxido de dioro.
Exemplos adicionais
-B2O3: óxido de boro; óxido bórico; ou trióxido de diboro.
-Cl2O7: óxido de cloro (VII); óxido perclórico; dicloro heptaxide.
-NO: óxido de azoto (II); óxido nítrico; monóxido de nitrogênio.
Referências
- Arrepio e Atkins. (2008). Química Inorgânica (quarta edição). Mc Graw Hill.
- Óxidos Metálicos e Não-Metálicos. Retirado de: chem.uiuc.edu
- Química Livre Online. (2018) Óxidos e Ozônio. Retirado de: freechemistryonline.com
- Toppr. (2018) Óxidos Simples. Retirado de: toppr.com
- Steven S. Zumdahl. (7 de maio de 2018) Óxido Enciclopédia Britânica. Retirado de: britannica.com
- Química LibreTexts. (24 de abril de 2018) Óxidos Retirado de: chem.libretexts.org
- Quimicas.net (2018). Exemplos de óxidos. Recuperado de: quimicas.net


