Óxido de Alumínio (Al2O3) Estrutura Química, Usos, Propriedades
O óxido de alumínio (Al2O3 de fórmula química), também chamado de alumina, óxido de alumínio, coríndon ou trióxido de alumínio, é um óxido de metal que é produzido a partir da reação entre um metal e oxigênio (O). É também conhecido como óxido básico, pela facilidade de formar hidróxidos quando reagem com a água.
Isso ocorre porque o alumínio que está na família IIIA da tabela periódica tem tendência a produzir os elétrons do último nível de energia. Essa tendência é devida à sua natureza metálica e sua baixa eletronegatividade (1,61 na escala de Pauling), que lhe confere propriedades eletropositivas e a converte em um cátion.

Em contraste, o oxigênio é um não-metal e é mais eletronegativo devido à sua alta eletronegatividade (3,44 na escala de Pauling). Portanto, ele tende a estabilizar a energia eletrônica de seu último nível, aceitando elétrons, o que faz dele um ânion.
As ligações formadas são ligações fortes, o que dá grande resistência ao óxido de alumínio. Na natureza, o alumínio não é encontrado na forma nativa, como ouro, prata, cobre, enxofre e carbono (diamante).
Isso significa que o alumínio não é combinado com nenhum outro elemento; Este metal é misturado com oxigênio, formando compostos como o corindo ou esmeril, que são compostos altamente resistentes e abrasivos.
Índice
- 1 fórmula e estrutura química
- 2 propriedades físicas
- 3 propriedades químicas
- 4 usos
- 5 referências
Fórmula e estrutura química
Fórmula Molecular: Al2O3
Fórmula estrutural: 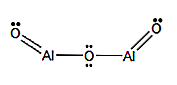
Propriedades físicas
- Está comercialmente disponível como um pó branco, inodoro e não tóxico.
- Como um composto mineral corresponde ao grupo de hematita. É um material muito duro que tem alta resistência ao desgaste, por isso é usado como material abrasivo.
- Conduz eletricidade facilmente e também é um bom condutor térmico.
- É resistente a reações com ácidos e bases a altas temperaturas.
- Pode aparecer em cores diferentes: vermelho ou rubi (onde os íons de alumínio foram substituídos por Cr3+), amarelo, rosa, safira azul, roxo, verde, cinza e incolor.
- Seu brilho é vítreo ou adamantino (diamante)
- Tem uma faixa branca muito delicada devido a sua dureza.
- Sua dureza na escala de Mohs é 9. Isso significa que ele pode arranhar outros minerais de menor dureza do que ele; no entanto, não pode arranhar o diamante que tem uma dureza de 10 na mesma escala.
- Sua densidade é de 3,96 g / cm3
- Seu peso molecular (massa molar) é de 101,96 g / mol.
- Seu ponto de fusão é 2040 ° C.
- Seu ponto de ebulição é 2977 ° C.
- É insolúvel em água.
Propriedades químicas
O óxido de alumínio não reage com a água a menos que esteja na presença de uma base forte.
No entanto, quando reage com ácidos, comporta-se como se fosse uma base:

Também mostra propriedades ácidas quando reagido com bases:

Embora a água não seja formada nesta reação, ela é considerada ácido-base porque Al2O3 neutraliza NaOH. Portanto, o Al2O3 É classificado como um óxido anfótero porque possui propriedades ácidas e básicas.
Na formação de alcenos e cicloalquenos, uma das formas mais utilizadas no meio industrial e laboratorial é através da desidratação de álcoois.
Para isso, o vapor de álcool é circulado em um catalisador quente de alumina ou óxido de alumínio (Al2O3); Neste caso, é considerado um ácido de Lewis.

Usos
- Alumina é usada na indústria para obter alumínio.
- É utilizado como material cerâmico devido à sua alta resistência à corrosão em altas temperaturas e desgaste.
- É usado como isolamento térmico, especialmente em células eletrolíticas.
- Tem capacidade para absorver água, o que a torna adequada para uso como agente de secagem.
- É utilizado como agente catalítico em reações químicas
- Devido à sua alta estabilidade térmica, é utilizado como oxidante em reações químicas que são realizadas em altas temperaturas.
- Previne a oxidação do catodo e terminais anódicos em uma célula eletrolítica.
- Devido à sua grande dureza e resistência, é utilizado em odontologia para a preparação de peças dentárias.
- É um bom isolante elétrico nas velas de ignição dos veículos que funcionam com gasolina.
- É amplamente utilizado em moinhos de bolas para a preparação de cerâmicas e esmaltes.
- Devido ao seu peso leve, nos processos de engenharia é usado para fazer aviões.
- Devido ao seu alto ponto de ebulição, ele é usado para fazer utensílios de cozinha, como frigideiras e refratários.
- É usado na instrumentação de máquinas de testes térmicos.
- Na indústria eletrônica, é utilizado na fabricação de componentes passivos para interconexão elétrica e na fabricação de resistores e capacitores.
- Utilizado na fabricação de enchimentos para soldagem.
- Óxido de alumínio é usado para o revestimento de óxido de titânio (pigmento usado para tintas e papéis de plástico).Isso evita reações entre o ambiente e esse tipo de pigmento, que não se decompõe ou enferruja.
- É usado como abrasivo em cremes dentais.
- É usado em hemodiálise.
- Como aditivo na indústria alimentícia, já que é utilizado como agente dispersante.
- É um agente antitranspirante de desodorantes.
- O óxido de alumínio tem sido usado como material ortopédico. Por ser um material inerte e poroso, o torna adequado para uso neste tipo de implante. Estes implantes permitem o crescimento fibrovascular, razão pela qual os fibroblastos e osteoblastos proliferam rapidamente neste material.
- O implante biocerâmico é feito com alumina. É leve e tem uma estrutura de poro uniforme muito bem interligada entre si. A estrutura microcristalina é mais suave do que a superfície áspera. Apresenta menos inflamabilidade após um período pós-operatório em comparação com outros materiais utilizados para implantes.
- Os flocos de óxido de alumínio produzem efeitos reflexivos dentro de tintas usadas para automóveis.
- Em algumas refinarias, o óxido de alumínio é usado para converter os gases tóxicos do sulfeto de hidrogênio em enxofre elementar.
- A forma de alumina chamada alumina ativada tem grandes benefícios no tratamento de águas residuais, tais como aqüíferos, devido à sua capacidade de adsorver muitos poluentes nocivos ao meio ambiente, bem como para filtrar resíduos que são dissolvidos na água e que é maior que o poro das folhas de alumina.
Referências
- Chang, R; Química, 1992, (quarta edição), México. McGraw-Hill Interamericana de México.
- Pine.S; Hendrickson, J; Cram, D; Hammond, G (1980), Química Orgânica(quarta edição), México, McGraw-Hill do México
- Kinjanjui, L., (s.f) Propriedades e usos do óxido de alumínio,Ainda funciona Recuperado, itstillworks.com
- Panjian L., Chikara, O., Tadashi, K., Kazuki, N., Naohiro, S., "e" Klaas de G., (1994). O papel da sílica hidratada, titânia e alumina na indução de apatita em implantes. Pesquisa de materiais do Journal of Biomedicals. Volume 18, pp. 7-15. DOI: 10.1002 / jbm.820280103.
- Guia Completo de Informações sobre Rochas, Minerais e Pedras Preciosas., Mineral.net., Recuperado, minerals.net
- LaNore, S. (2017), Características Físicas do Óxido de Alumínio, Sciencing,Recuperado, sciencing.com



